近日,我校史俊峰教授团队与曾湘祥教授团队在国际知名学术期刊《Nature Communications》上发表了题为“A Foundation Model Identifies Broad-Spectrum Antimicrobial Peptides against Drug-Resistant Bacterial Infection”的研究论文。该研究开发了一种全新的抗菌肽发现基础模型——deepAMP,并成功设计出多个可与抗生素媲美的广谱抗菌肽,为应对日益严重的抗生素耐药性危机提供了新的思路和方法。
耐药性细菌感染是当前最严重的公共卫生问题之一,每年导致约70万人死亡,预计到2050年,这一数字将上升至1000万。然而,在过去几十年中,鲜有新型抗生素被发现并投入临床使用,而且由于这些新抗生素的结构由于与已知的较老抗生素相似,细菌会很快适应并产生耐药性。因此,研发具有全新结构的抗生素尤为迫切。抗菌肽是一类由10至50个氨基酸组成的阳离子、两亲性短肽,其独特的膜损伤抗菌机制不易诱导细菌产生耐药性,因此被视为后抗生素时代理想的抗生素替代品。然而,抗菌肽可能的序列组合数量极为庞大。例如,仅考虑20种天然氨基酸的情况下,一个20肽就有1020种不同的组合可能性,要想从中找到有效的抗菌肽无疑像大海捞针一样困难。
为了快速生成和识别高活性的抗菌肽以应对抗生素耐药危机,我校史俊峰教授团队与曾湘祥教授团队联合研发了一个基于肽语言的深度生成框架(deepAMP),它包括生成和预测两大部分。与现有的计算方法相比,deepAMP模型在识别有效抗菌肽方面展现出更高的准确性和可靠性。实验结果表明,该模型生成高活性候选抗菌肽的成功率超过90%。这些候选抗菌肽主要通过增强细菌外膜的渗透性以及破坏细菌的细胞膜结构来发挥抗菌作用,这种物理性破坏使细菌难以通过突变单一的蛋白或者酶来产生耐药性。通过构建小鼠真皮伤口感染模型进行测试,发现其中三条候选抗菌肽的体内抗感染疗效与抗生素左氧氟沙星相媲美,并且不易诱导细菌产生耐药性。
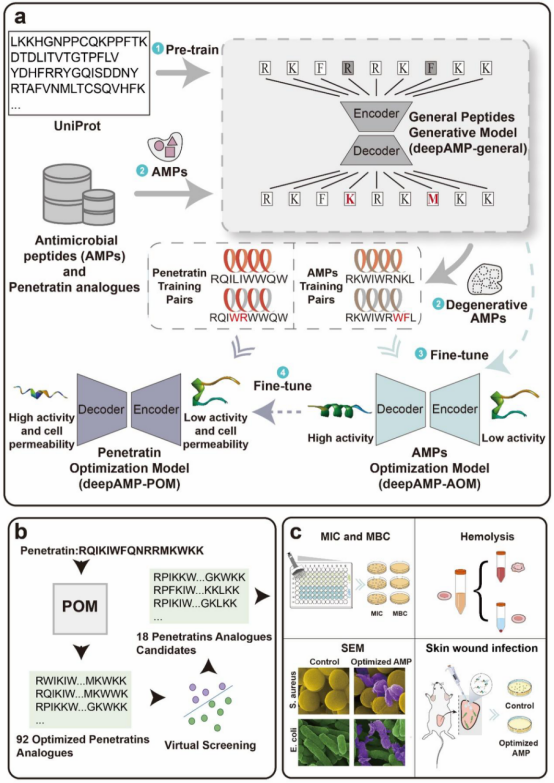
deepAMP模型的工作流程图