N6-甲基腺嘌呤(N6-methyladenosine,m6A)是真核生物mRNA中最丰富的内部修饰,在调节RNA功能和代谢方面起着关键作用。METTL3-METTL14甲基转移酶复合物是负责催化m6A的关键元件,包括催化亚基METTL3和辅助亚基METTL14,以及多个支架蛋白WTAP、ZC3H13和RBM15等。METTL3作为METTL3/14甲基转移酶复合物中重要的催化核心,已被鉴定为多种肿瘤潜在的治疗靶点。
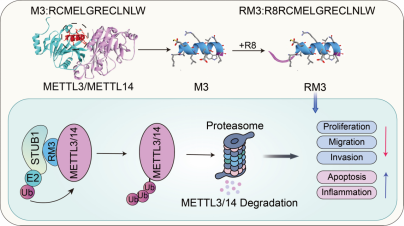
近日,湖南大学生命交叉研究院史俊峰课题组在Angewandte Chemie International Edition发表了一篇题为Peptide degrader-based targeting of METTL3/14 improves immunotherapy response in cutaneous melanoma的研究论文。该研究验证了METTL3在恶性黑色素瘤发生发展中的促进作用,并对课题组前期开发的靶向METTL3的多肽抑制剂RM3的作用机制进行了进一步挖掘。结果表明RM3能够招募E3连接酶STUB1降解并通过蛋白酶体途径降解METTL3,并重塑肿瘤微环境以增强肿瘤对免疫检查点抑制剂的应答。后续一系列实验也证实RM3不仅能够有效抑制黑色素瘤生长,而且能够改善免疫治疗的效果,并具有良好的安全性。

该研究首先构建了METTL3稳定敲低的黑色素瘤细胞系,通过EdU掺入,Transwell和细胞成球等实验,证实了METTL3能够促进黑色素瘤细胞的增殖,迁移,侵袭和自我更新能力;同时荷瘤实验进一步证实METTL3能够促进黑色素瘤的体内生长。上述结果表明METTL3在黑色素瘤中发挥促癌功能。
在此基础上,利用亲和力测定和多肽pull down等实验,证实了RM3能够有效具有靶向METTL3。同时通过细胞毒性和Western blot实验,证实RM3能够有效降低黑色素瘤细胞活性,并诱导METTL3和METTL14的降解。为了阐明RM3诱导METTL3/14降解的潜在机制,作者进行了蛋白半衰期实验,发现RM3能够缩短METTL3半衰期;进一步通过网站预测,IP实验和泛素化实验,证实RM3的处理能够招募更多的STUB1,提高METTL3与METTL14的泛素化水平进而诱导其降解。与此同时,RNA-seq数据表明RM3的处理可能重塑肿瘤微环境中的炎性反应,增强肿瘤对免疫检查点抑制剂治疗的反答。
接下来,体外细胞实验表明对RM3处理后黑色素瘤细胞的增殖,迁移和侵袭能力降低,并诱导黑色素瘤细胞的凋亡。而且小鼠荷瘤模型也证明RM3能够有效抑制黑色素瘤的体内生长,并具有较好的安全性。更重要的是,RM3与aPD-1的联合治疗组的治疗效果更优于单药治疗组,表明RM3能够提高免疫治疗的应答反应。
综上,该研究不仅证实METTL3在黑色素瘤中的致癌作用,而且表明RM3作为METTL3的多肽降解剂,可以作为一种有前景的肿瘤治疗策略和联合治疗选择。
湖南大学生命医学交叉研究院博士生韩宏和李增辉为本论文的共同第一作者,史俊峰教授为通讯作者。课题组在多肽药物领域持续发力,近3年在Nat.Commun(2024)、Angew Chem (2022, 2024, 2024)、ACS Nano (2023)、J. Control. Release (2024) 等国际期刊发表高水平论文16篇,申请或获批专利15个。课题组经费充足,欢迎有志于多肽研究的青年才俊加入课题组从事博士后研究。